Die quantitative Bestimmung von Nickel und Cobalt basiert auf der adsorptiven Anreicherung des Dimethylglyoximkomplexes an der stationären Quecksilberelektrode (Kapitel 5.2). Anschließend wird das Nickel dann in adsorbierter Form als bis-(Dimethyl-glyoximato)nickel(II) reduziert. Der geschwindigkeits-bestimmende Schritt ist die Übertragung des zweiten Elektrons an die adsorbierte Zwischenverbindung mit deren gleichzeitiger Protonierung. Durch die Reduktion des Zentralions zerfällt die Chelatverbindung [116].
Im Vergleich zu Zn, Cd, Pb und Cu, die in Quecksilber löslich sind, und deren Oxidationsstrom durch die Diffusion kontrolliert wird, ist der gemessene Strom für Nickel und Cobalt bei gleichen Anreicherungszeiten wesentlich höher.
Das von PILHAR et al (1981) [59] vorgestellte “Verfahren zur voltammetrischen Bestimmung von Nickel bei der Routineanalyse von Wasser, biologischem Material und Lebensmitteln“ mittels Gleichspannungs- oder differentieller Pulsvoltammetrie verwendet ebenso wie die von OSTAPCZUK et al (1986) [114] vorgestellte Methode zur Nickelbestimmung mittels SWV einen 0,1 M Ammoniumpuffer (pH 9,2 ± 0,2) als Leitelektrolyt für Ni(II)-Konzentrationen bis 10 µg/l bzw. einen 1 M Ammoniumpuffer bis Ni(II)-Konzentrationen von 1 mg/l.
Für die Bestimmung von Nickel in biologischen Materialien oder Lebensmitteln wurde folgende Prozedur [59] ausgearbeitet: Die Probelösung wird nach Aufschluß mit NH3 (25%) neutralisiert und ein Aliquot in die Zelle pipettiert. In die Zelle werden vorher 0,1 M Ammoniumpuffer und 1 · 10-4 M DMG vorgelegt.
Bei manueller Versuchsdurchführung war der Ammoniumpuffer, der nach PILHAR et al aus gleichen Teilen NH3 (25%) und HCl (30%) hergestellt und während der Analyse fest verschlossen blieb, über lange Zeit stabil. Der Ammoniumpuffer gewährleistete bei gleichartigen Aufschlußlösungen eine sichere Einstellung des pH-Wertes mit einheitlichen Puffervolumina.
Diese Vorgehensweise erwies sich jedoch für die vollautomatische Durchführung der voltammetrischen Analyse als nicht praktikabel. Da der Puffer bei großen Meßreihen über eine lange Zeit für den Autosampler bereitgestellt werden mußte, konnte das Gefäß mit dem Puffer nicht fest verschlossen werden. Dies hatte zur Folge, daß Ammoniak aus dem Puffer entwich und Proben nach längerer Standzeit nicht mehr ausreichend neutralisiert und auf den angestrebten pH-Wert eingestellt werden konnten.
Es wurden daher zwei getrennte Pufferlösungen aus 4M NH4Cl und 4M NaOH hergestellt, die erst mittels Autosampler im Verhältnis 2:1 in die Meßzelle mit der vorgelegten Probelösung gelangten. Das Puffervolumen sowie die in der NaOH-Lösung enthaltene DMG-Konzentration wurde innerhalb einer Meßreihe des gleichen Probentyps an die Probenvorbereitung und die entsprechende Acidität angepaßt. Die sauren Probelösungen konnten somit sicher neutralisiert und auf den angestrebten pH-Wert von 9,2 eingestellt werden, wodurch eine vollautomatische Abarbeitung aller Analysenproben im Standardadditions-verfahren ermöglicht wird.
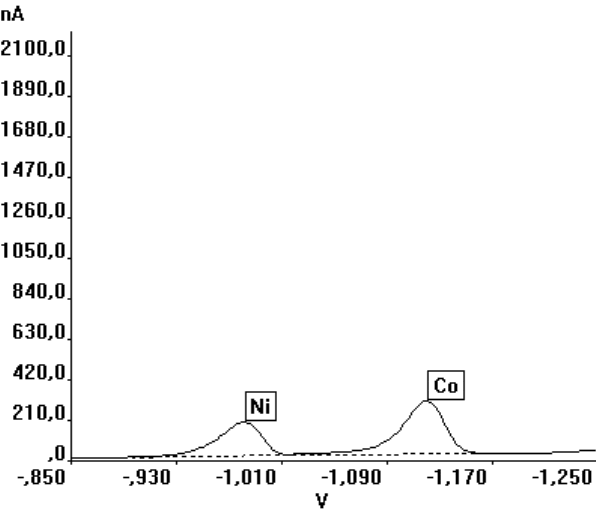
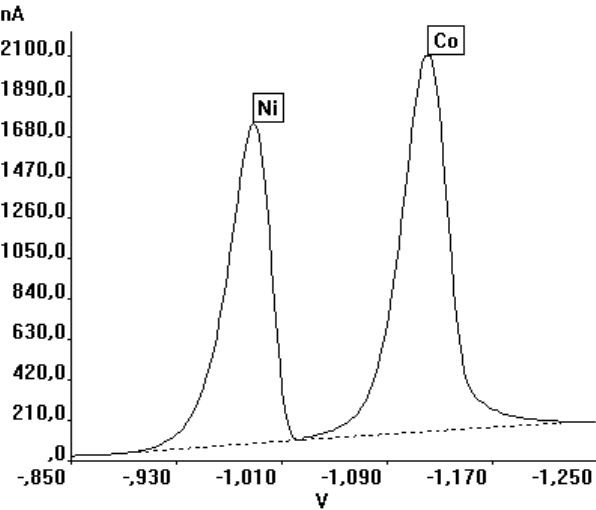
Bei dieser adsorptiven Anreicherung von Chelatverbindungen kann aus den in Kapitel 5.3 geschilderten Gründen die SWV mit hohem Spannungsvorschub besonders vorteilhaft eingesetzt werden. Die Empfindlichkeit für Ni konnte durch die Anwendung der SWV um den Faktor 11, für Co um Faktor 6 gegenüber dem DP-Modus bei gleichen Meßbedingungen und einer Pufferkonzentration für Aufschlußlösungen biologischer Materialien gesteigert werden (s. Abb. 39).
| a) DP | b) SWV | |
 |
 |
|
Abb.39 Vergleich der Signale für Ni und Co im DP- und SWV-Modus, CCo, Ni: 1 µg/l, |
||
Durch die beobachtete Empfindlichkeitssteigerung der SWV gegenüber dem DP-Modus konnte eine ausreichende Nachweisgrenze selbst im Ultraspurenbereich bereits bei Anreicherungszeiten von 60 bis 180 Sekunden erzielt werden.
Ein Änderung der SW-Pulsamplitude (ESW) kann sich auch hier (s. 9.2.2) auf die Empfindlichkeit und das Auflösungsvermögen der Elementsignale auswirken.
| a) ESW = 5 mV | b) ESW= 50 mv | c) ESW = 100 mV | ||
 |
||||
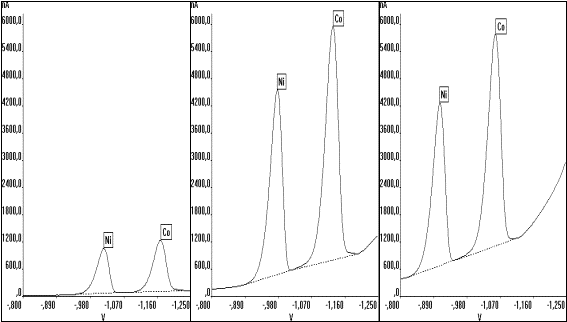
Abb.40 Einfluß der SW-Amplitude (ESW)
auf die Elementsignale; CCo, Ni: 10 µg/l, |
||||
Eine Erhöhung der SW-Amplitude führt zu einem Anstieg des Untergrunds und zu Signalüberlappungen, wodurch die Empfindlichkeit mit zunehmender Amplitude wieder abnimmt (Abb.40).
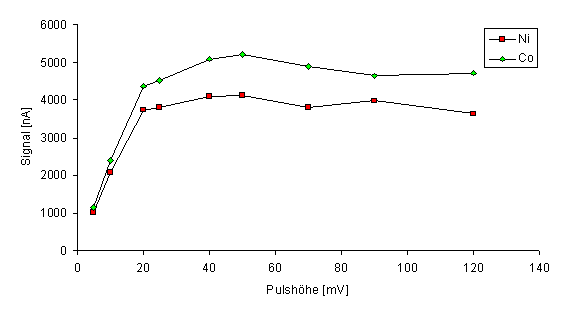 |
Abb.41 Einfluß der SW-Amplitude (ESW) auf die Elementsignale; CCo, Ni:
10 µg/l, |
Eine Pulshöhe (ESW) von 50 mV bei einer Frequenz von 100 Hz führte zu der größten Empfindlichkeit bei vertretbarem Untergrund (s. Abb.41).
[116] Pilhar, B.; Valenta, P.; Nürnberg, H.: Elektrochemical reduction of Ni(II) on the HMDE in the Presence of Dimethylglyoxime, J. Elektroanal. Chem., 214 (1986) 157-177.